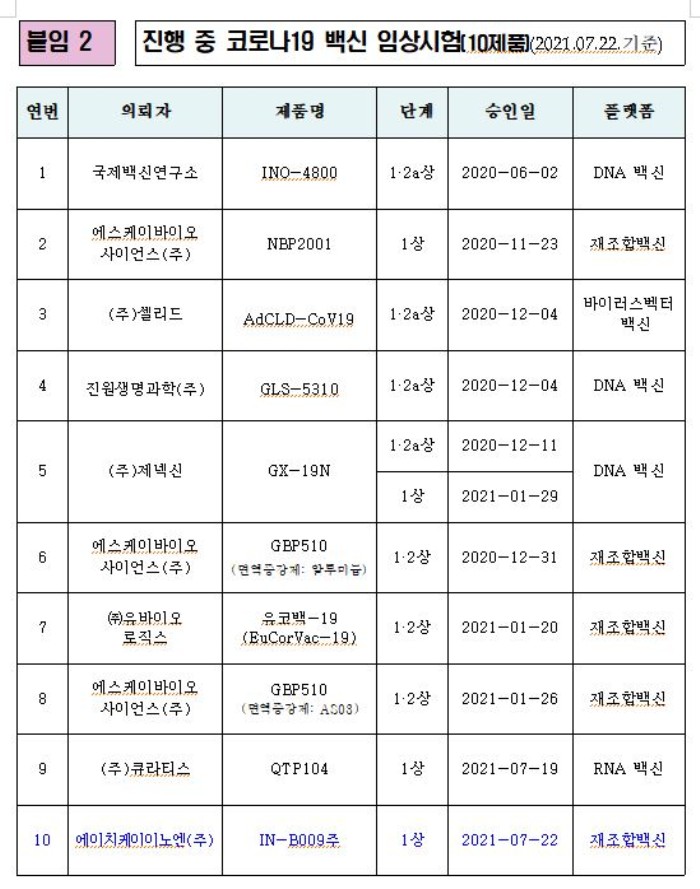
식품의약품안전처는 국내 개발 코로나19 백신 ‘IN-B009주’(에이치케이이노엔(주))의 안전성과 면역원성을 평가하기 위한 임상 1상 시험 계획을 7월 22일자로 승인했다.
이번 승인으로 국내에서 코로나19 관련해 임상시험을 진행하고 있는 의약품은 백신 10개, 치료제 13개(11개 성분) 등 총 23개 제품이다.
‘IN-B009주’는 코로나19 바이러스의 ‘표면항원 단백질’을 유전자 재조합 기술로 만든 ‘재조합 백신’이다. 특히 이번에 승인받은 백신은 표면항원 단백질의 N-말단 부위에 세포 투과 펩타이드(Cell Penetrating Peptide, CPP)를 추가로 발현시켜 세포 내로 단백질이 잘 전달될 수 있도록 개발됐다.
한편 해외에서도 미국 노바백스(3상) 등이 유전자재조합 기술을 이용한 코로나19 백신의 임상시험을 진행하고 있다.
식약처는 앞으로도 국민적 관심이 높은 코로나19 치료제·백신 개발 제품의 임상시험 현황에 대한 정보를 신속하게 전달하는 한편 안전하고 효과 있는 코로나19 치료제·백신 개발을 지원해 우리 국민이 질병을 예방하고 치료 기회를 보장받을 수 있도록 최선을 다한다는 방침이다.